AI行业资讯第十八期:Nature发布医疗AI突破性成果;DeepSeek新奖励模型铺垫R2;英伟达联合谷歌、迪士尼推出新引擎
发表日期: 2025年5月12日
4月,Nature发布了一项新研究,介绍了一种专为临床诊断推理优化的大型语言模型——Articulate Medical Intelligence Explorer(AMIE)。该研究强调,准确诊断对有效医疗至关重要,但开发能够辅助医生进行诊断的人工智能(AI)系统一直充满挑战。传统研究多关注机器输出诊断的准确性,然而,实际临床实践需要一个迭代且互动的推理过程。AMIE的问世为设计新型交互工具带来了转机。

论文链接:


四、DeepSeek-R2即将到来,清华合作推动奖励模型新进展
4月5日,DeepSeek发布了一篇新论文,与清华大学研究者合作揭示了一种全新的奖励模型推理Scaling方法。研究指出,尽管强化学习可以有效提升大型语言模型的推理能力,但在多个领域中获取准确的奖励信号仍是一个重大挑战。为解决这一问题,DeepSeek与清华研究团队提出了一种名为自我原则点评调优(Self-Principled Critique Tuning, SPCT)的创新学习方法,并基于此构建了DeepSeek-GRM系列模型,同时引入元奖励模型(meta RM)进一步优化推理扩展性能。

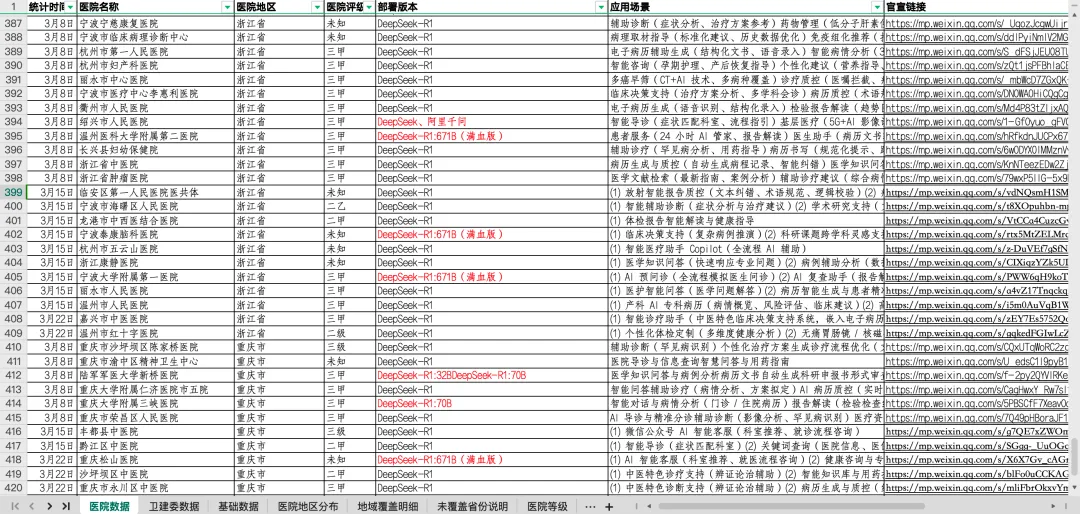
五、AI+医疗,DeepSeek赋能420余家医院最新数据
3月25日最新发布的数据展示了DeepSeek在医疗领域的多场景应用情况。这些应用基于420余家医院的实践成果,展现了AI在提升医疗服务质量与效率方面的潜力。
https://mp.weixin.qq.com/s/WfWaRbackd3J533cZnoiog
近日,英伟达联合多家机构推出的VISTA3D多模态医学影像分割模型,凭借其首创的三维超体素特征提取方法,实现了三维自动分割与交互式分割双模态的协同优化。在23个数据集的综合基准测试中,该模型的分割精度较现有最优专家模型提升了5.2%。

https://doi.org/10.48550/arxiv.2406.05285